【시사매일닷컴 김용환 기자】식품의약품안전처는 의료기기 개발지원을 위한 사전검토 대상 품목을 확대하고 사전검토 자료의 범위를 확대·세분화하는 내용을 담은 의료제품 사전검토 운영에 관한 규정 개정안을 14일 행정예고하고 다음달 4일까지 의견을 받는다고 14일 밝혔다.
의료기기 개발지원을 위한 사전검토는 품목허가·신고·인증 또는 임상시험계획 승인 등에 필요한 자료에 대해 식약처에 미리 검토받을 수 있는 제도를 말한다. 이번 개정안은 보건·산업상 가치가 있는 희소·혁신 의료기기 등에 대해 사전검토 제도를 확대·활성화함으로써 허가·심사 시 제출자료 미흡 등으로 인한 허가 지연을 줄여 신속한 제품화에 도움을 주고자 마련했다.
사전검토 대상 확대로 연간 약 380건 이상이 제품화 기간 단축이 예상된다. 참고로 이번 제도개선은 식약처 내부 끝장토론, 산업계·협회·학계 등과 간담회·토론회를 거쳐 8월 11일 발표한 ‘식의약 규제혁신 100대 과제’ 추진의 일환이다.
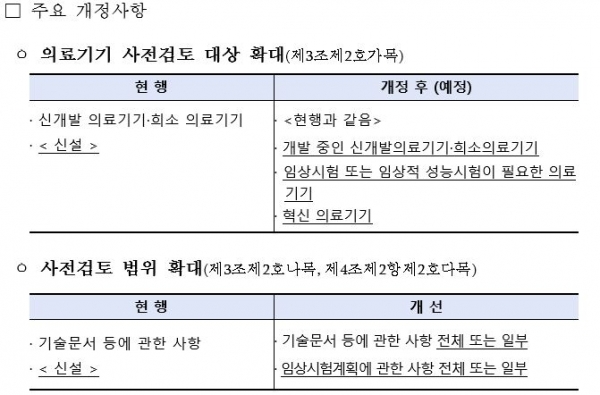
식약처에 따르면 의료기기 사전검토 대상 확대를 위해 그간 신개발 의료기기·희소 의료기기에 한정해 사전검토 제도를 운영하던 것을 앞으로는 △개발 중인 신개발 의료기기·희소 의료기기 △임상시험(임상적 성능시험 포함) 자료 제출이 필요한 의료기기(임상시험용 의료기기 포함) △혁신 의료기기까지 확대한다.
△신개발 의료기기는 이미 허가(인증)받거나 신고한 품목과 비교해 사용목적, 작용원리, 원재료, 성능, 사용 방법이 완전히 새로운 의료기기로 품목(인증)시 인정 △희소 의료기기는 희귀질환 진단·치료에 사용되며 국내에 대체할 수 있는 제품이 없는 의료기기 △혁신 의료기기는 기존 의료기기나 치료법에 비해 안전성·유효성이 현저히 개선 또는 개선할 것으로 예상되는 의료기기△임상시험용 의료기기: 임상시험계획 승인을 이미 받았거나 받고자 하는 의료기기 등이다.
또한, 의료기기 사전검토 자료 범위 확대·세분화를 위해 현행 사전검토 자료의 범위는 제품화 단계에서 품목허가 신청 시 제출하는 ‘기술문서 등에 관한 자료’로 한정했으나 앞으로는 허가 신청 전 단계인 임상시험 실시 승인에 필요한 ‘임상시험계획(임상적 성능시험계획 포함) 승인에 관한 자료’까지 확대한다.
아울러 현재 ‘기술문서 등에 관한 자료’ 등 전체를 사전검토 자료로 규정하고 있으나, 앞으로는 일부 자료만으로도 사전검토를 신청할 수 있도록 세분화된다.
식약처는 "이번 개정으로 국민 안전을 최우선으로 효과적인 혁신 의료기기 등이 제품화되는 기간이 단축되고 의료 현장에서 의료기기를 신속히 사용할 수 있게 돼 환자의 치료 기회 확대로 이어질 것으로 기대되고 앞으로도 의료제품의 경쟁력 강화를 위해 적극적으로 규제를 개선할 것"이라고 밝혔다.
